執筆:弁護士 早崎 智久(メディカル・ビューティー・ヘルスケアチーム)
(※2022年8月31日に公開。2024年6月12日に記事内容をアップデートいたしました。)
2022年8月31日 公開
2024年6月12日更新
連載:薬機法とは ~薬機法の基本~
『第1回 薬機法の全体像』はこちらから
『第2回 「医薬品等」とは』はこちらから
『第3回 医薬品の販売と薬局 ① -医薬品の種類-』はこちらから
『第4回 医薬品の販売と薬局② -医薬品の販売と薬局-』はこちらから
『第5回 医薬品の製造販売① -全体像と製造販売業・製造業・製造管理-』はこちらから
『第6回 医薬品の製造販売② -医薬品の製造販売承認-』はこちらから
『第7回 製造販売後の医薬品 -医薬品の安全管理と有効性の再確認-』はこちらから
『第8回 医薬品情報の消費者への表示-医薬品の表示、添付文書、広告-』はこちらから
1.はじめに
GVA法律事務所では、メディカル、美容、ヘルスケア領域に関して専門チームを設け、各分野について多様なサポートをさせていただいております。
薬機法の基本に関する連載3回目と4回目は、医薬品の販売と薬局に関してご説明しました。5回目となる今回と次回は、医薬品を市場に流通させることに関する規制について解説いたします。
医薬品の製造販売業、製造業にかかわる方、製造販売と製造の違いがわからずに困っている方、ルールの全体像を理解したい方に向けた記事なので、ぜひ最後までお読みください。
2.医薬品を市場に流通させるための規制の全体像
前々回と前回は、医薬品の販売と薬局についてご説明いたしました。これは、私たちが医薬品を購入したり、処方されたりする場面から、医薬品がどのような規制のもとで販売されているのか、処方されているのかを見て参りました。
今回は、「では、その購入する医薬品はどのように市場に供給されるのか?」という視点から見ていきたいと思います。
まず、医薬品もモノですので、他のモノと同じように、製造されたり外国から輸入された後に、前回見た医薬品卸売販売業者、薬局などを経て、病院・診療所や薬局、店舗などに納品され、患者や一般人の手元に届くことになります。
しかし、医薬品が通常のモノと異なるのは、「医薬品は、作りたい、輸入したいと思っても、自由に製造したり、輸入したりできない」ということです。
医薬品は、他のモノと異なり、人体に使用するものです。同様に人体に関わるものとして食品についても規制が設けられていますが、医薬品は食品と比較しても人体への影響が大きい(副作用など)ため、厳しい規制がかけられています。様々な試験を経た結果、「これなら医薬品として流通させてもよろしい」とならなければ、作ったり、輸入すること自体が許されないものになります。
さらに、ややこしいのは、「この製品なら医薬品として流通させてもよろしい」というのは、あくまで、その医薬品自体に関してのものです。通常であれば、日本は自由競争の国ですから、「他の会社の製品が売れているから、私もこれと同じようなものを流通させよう」と言って流通させることに問題はありません(他社の知的財産権を侵害してはいけないのはもちろんですが)。実際に、食品も飲料も洋服も机もスマートフォンもPCも、社会のたくさんのモノが、様々な会社によって作られたり、輸入されたりしています。しかし、医薬品については、「この医薬品を流通させていいなら、私もやろう」と思っても、直ちにはやれません。流通させようと思っている者についても、「あなたならこの医薬品を市場に流通させてもよろしい」とならなければ、医薬品を流通(これを「製造販売」といい、詳細は後述します。)させられないのです。
つまり、医薬品については、
① 医薬品自体の製造販売に対する承認
② 医薬品を製造販売しようとする事業者に対する許可
の2つの規制があります。
以下、この①と②の概要をご説明しますが、分かりやすさの点から、②、①の順にご説明します。
3.医薬品の製造販売に関する規制の概要
⑴ 製造販売しようとする事業者に対する許可
前述のように、医薬品として製造したり、輸入したりしようとする場合、「あなたなら、この医薬品を流通させてもよろしい」という許可が必要になります。この許可を「製造販売業の許可」といいます。
ここで、まずは、この「製造販売」という言葉を確認しましょう。
この「製造販売」には、製造と販売という2つの言葉が入っているため、前回までに見てきた「医薬品の販売」と何が違うのか?となりますが、薬機法においては全く別の用語であり、「製造販売」という一つの言葉として理解することが重要です。
薬機法を見ますと、医薬品の「製造販売」は以下のように定義されています。
薬機法第2条第13項
この法律で「製造販売」とは、その製造(他に委託して製造をする場合を含み、他から委託を受けて製造をする場合を除く。以下「製造等」という。)をし、又は輸入をした医薬品(原薬たる医薬品を除く。)、医薬部外品、化粧品、医療機器若しくは再生医療等製品を、それぞれ販売し、貸与し、若しくは授与し、又は医療機器プログラム(医療機器のうちプログラムであるものをいう。以下同じ。)を電気通信回線を通じて提供することをいう。
これを整理すると、
① 自ら製造した医薬品を販売、貸与、授与すること
② 他の業者に委託して製造した医薬品を販売、貸与、授与すること
③ 輸入をした医薬品を販売、貸与、授与すること
の3つの場合が含まれ、これらを総称して「製造販売」といいます。
このように見ると、「製造販売」は、前回までに見た「販売」とは違うものであることが分かります。
つまり、前回までに見た「販売」というのは、市場に流通された医薬品を、医療機関や一般人に販売することを意味しますが、「製造販売」というのは、医薬品をそのような流通に乗せる行為ということになります。
ポイントとしては、「製造販売」は、他の業者に製造してもらうことや輸入することを含んでいるということです。すなわち、製造販売事業者というのは、「医薬品を日本市場に流通させる者がその医薬品について最終責任を負う」ということになりますので、自ら製造する場合に限らず、他者に製造してもらう場合や、外国の業者が製造したものを輸入することも含むのです。
このことから、「製造販売」と「製造」とが、異なる意味を持つことも分かります。医薬品を実際に製造することは「製造」といいますが、「製造販売」は、上記のように製造することではなく、医薬品を流通させることを意味するものですので、全く別の概念です。
製造販売≠製造、販売 この「製造販売」するための許可、つまり、「あなたならこの医薬品を流通させてもよろしい」という許可のことを、「製造販売業の許可」といいます。一方、医薬品を製造するための許可、つまり「あなたならこの医薬品を作ってもよろしい」という許可のことを「製造業の許可」といいます。
このように、「製造販売」と「製造」は、別のものとして、別々の許可が必要になります。そのため、仮に、自ら医薬品を製造した上で、その医薬品を市場に流通させる場合は、製造業の許可と製造販売業の許可の2つの許可が必要になります。
これらの詳細については、本記事において後述します。
⑵ 医薬品自体に対する製造販売の承認
次に、医薬品自体に対する承認、つまり、「この医薬品なら、市場に流通させてもよろしい」ということについてご説明します。
前述のように、医薬品は、人体への影響が大きいモノなので、勝手に流通させることは禁止されています。正式に承認された医薬品にも副作用はありますが、副作用の程度を超えて人体に害を与えてしまうことを「薬害」といいます。薬害の原因は様々であり、製造段階における問題から生じたものもありますが、医薬品自体の安全性の審査が不十分、つまり「この医薬品なら」という点の審査のミスにより生じたものもあります。1960年代に多くの被害者を生んでしまったキノホルム製剤によるスモンや、同じ時期のサリドマイドによる胎児への障害などはその代表例で、国は、そのような悲劇が起きないように、それまで以上に厳しい審査を行うようになりました。
また、仮に薬害が発生しない場合も、何の効き目もないような医薬品(効能効果の無い医薬品)を流通させるわけにもいきません。また、効能効果もあり、副作用の問題が小さくても、すぐにボロボロになったり、その結果効能効果がなくなるような、医薬品の形状等が問題になるような品質の悪い医薬品も問題です。
以上から、医薬品には、安全性、効能効果、品質の全てにおいて、問題のないことが求められ、そのような製品でなければ、市場に流通させることはできません。
そして、この問題のないことをデータに基づいて説明できた場合に限り、国は、その製品を「医薬品」として流通させるものとしており、これが「医薬品の製造販売の承認」という制度になります。この承認については、次回、詳細にご説明します。
医薬品を自社で製造販売する場合にどんなことが問題になりそうか、どんなことに注意すればよいのか、など、確認したい、知りたい方は、初回30分無料相談で対応しておりますので、お気軽にお声掛け下さい。
4.医薬品の製造販売業
まず、医薬品の製造販売業について見ていきます。
⑴ 製造販売業の概要
前述のとおり、医薬品を市場で流通させるためには、事業者が製造販売業の許可を得ることが必要です。そして、薬機法においては、その医薬品に関わる責任は、製造販売業者が負うものとしています。
つまり、「あなたならこの医薬品を流通させてもいいけれど(許可)、その代わり、この医薬品がちゃんとした品質管理のもとで製造されているかどうか、市場に流通した後も安全性に問題が起きていないかどうかを責任をもって監督しなさい」というのが、「製造販売業の許可」ということになります。
⑵ 製造販売業の許可基準(薬機法第12条、第12条の2)
そこで、この「許可」を得るために何が必要になるかを見ていきますが、上記のように、製造販売業者に求められるのは、①医薬品の「品質管理」と②医薬品の「市場流通後の安全管理」の2つです。そのため、許可の基準も、申請者がこの2つのことをできるかどうかという点から行われます。
この基準ですが、以下のように、厚生労働省の省令としてまとめられています。
① 品質管理の基準
=『医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準に関する省令』
(通称「GQP省令」=Good Quality Practice)
② 製造販売後の安全管理の基準
=『医薬品、医薬部外品、化粧品、医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令』
(通称「GVP省令」=Good Vigilance Practice)
(なお、薬機法に関連する省令では「G〇P省令」というものが複数あり、最初は区別がつかないと思われる人も多いかと思いますが、品質(Quality)管理の「Q」と、(安全性を)警戒・用心(Vigilance)して管理するの「V」とだけ理解しておけば、省令の役割・内容と通称に迷うことはありません。)
この2つの基準が求める内容をすべて満たし、欠格事由(法第12条の2)に該当しなければ、許可されます。
また、取得した許可は永久に有効というものではなく、第一種医薬品製造販売業、第二種医薬品製造販売業のいずれも「5年」とされていますので、その都度の更新が必要になります。
なお、この「品質管理」については、製造販売と製造のいずれにも関わるものなので、製造業に関するご説明をした後に本稿の「6」でご説明し、「製造販売後(市場流通後)の安全管理」については、別の機会にご説明する予定です。
⑶ 製造販売業者における責任者
製造販売業の許可は、法人・個人のいずれでも得ることができますが、その責任を実際に果たしていくのは人なので、特別な役職が必要とされます。これが、医薬品等総括製造販売責任者(総責)、品質保証責任者(品責)、安全管理責任者(安責)であり、いわゆる「三役」です。
医薬品の場合、総括製造販売責任者は、原則として薬剤師の資格を有する者から選任する必要があります(厚生労働省令で定める医薬品のみを製造販売する場合と困難な事情がある場合は例外です)。
医薬品総括製造販売責任者は、品質管理と安全管理の2つについて、総括して管理して指示する者であり、必要な時は、製造販売業者に対してその意見を書面で述べる義務を負います。そして、この総責の管理・指示のもと、品質保証責任者が品質保証部門で、安全管理責任者が販売後の安全管理部門で、それぞれ業務を行うことになります。
⑷ 医薬品製造販売業の種類
薬機法第12条を見ると、医薬品の製造販売業の許可は、第一種医薬品製造販売業と第二種医薬品製造販売業の2種類に分かれています。
これは、以前に医薬品の種類において確認したように、医薬品は、その副作用の程度などに応じて、多数の種類に分かれているところ、特に、市場流通後の安全管理の必要性は、副作用が強い医薬品においてはより厳格に行われる必要があります。そこで、特に副作用の強いと考えられる処方箋医薬品については、他の医薬品と区別し、第一種医薬品製造販売業として、より厳しい義務を課しているのです。
なお、第一種医薬品製造販売業は処方箋医薬品の製造販売しかできませんので、その他の市販薬などを製造販売するためには、第二種医薬品製造販売業の許可も取得することが必要になります。
5.医薬品の製造業の許可
次に、医薬品の製造業について見ていきます。
⑴ 医薬品製造業の概要
前述のように、製造業の許可というのは、文字どおり、医薬品を「製造」するための許可になります。そのため、医薬品を市場に流通させるために製造販売業の許可を得ている者が、自ら工場で製造する場合は、別に「製造業の許可」を取得する必要がありますし、製造販売業者から委託されて製造だけ行う場合も、許可の取得が必要になります。
そして、この「製造」については、実際に製造が行われる場所ごとに、きちんとした設備や体制のもとで品質に問題のない製品が「製造」されるかどうかが重要になりますので、「製造所」ごとに許可が必要となります。そのため、例えば、ある業者が、A工場で医薬品を精製し、B工場で包装し、C工場で保管をする場合は、A、B、Cの全ての工場ごとに原則として製造業の許可が必要になります。
⑵ 医薬品製造業の種類(許可の区分)
医薬品製造業が文字通り医薬品の「製造」を行うことは前述しましたが、この「製造」という行為には、多数の工程が含まれています。そして、すべての医薬品製造業者が、そのすべてを単独で行うものではありません。
例えば、製造販売業者が海外から輸入した医薬品製品に対して、日本語のラベルを貼ることも「製造」の一部です。
また、製造販売業が医薬品の種類に応じて2種類に分かれていたように、製造業においても、医薬品の副作用の程度などに応じて、製造において必要な注意の程度も異なります。
そのため、医薬品製造業の許可は、以下の5つの区分に分かれています。
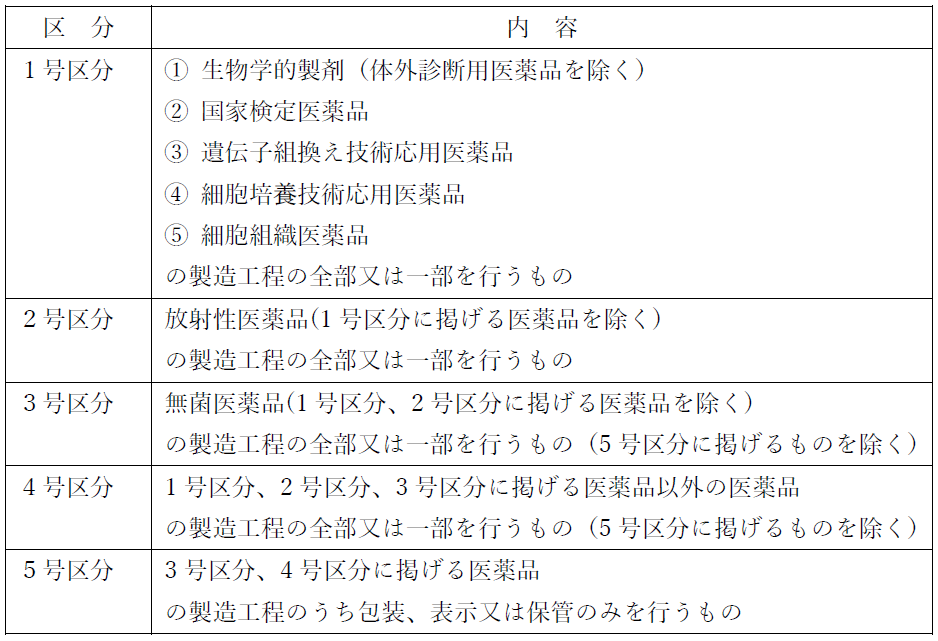
⑶ 「登録」で足りる医薬品製造業(保管のみを行う場合)
なお、上記⑵の「5号区分」では、保管のみを行う業者が含まれますが、特に品質管理上の問題が少ない場合においては、厳格な許可までは必要ないともいえます。
そのため、令和3年8月1日の薬機法改正により、問題の少ない保管のみを行う「製造業の登録」制度が新たに設けられました。
問題が少ないとされたのは、以下の4つの条件の全てを満たす場合です。
① 保管(保管のために必要な検査等を含む。)のみを行う製造所であること
② 包装、表示その他の製造行為又は試験検査(当該製造業者の他の試験検査設備又は他の試験検査機関を利用して行う場合を含む。)を行う製造所ではないこと
③ 最終製品(他の製造所に出荷されるものを除く。)の保管を行う製造所ではないこと
④ 保管の対象が厳格な取扱いが必要になる生物学的製剤などの特別な医薬品ではないこと※この医薬品の詳細は薬生薬審発0428第2号令和3年4月28日「医薬品等の保管のみを行う製造所の取扱い等について」に定められています。この内、①と②は「保管」だけを行うということから当然のことですし、④も、慎重な取り扱いが必要な医薬品であること求められます。そして、③については、最終製品の場合は市場流通までの最終段階にあり、慎重な管理が必要なことから除外されています。
⑷ 製造業の許可基準
ア 製造業の許可基準
製造業販売業に関するところでご説明したように、医薬品を市場に流通させることに関する責任を負うのは製造販売業者とされています。この内、品質管理についての基準を定めたものが前述の「GQP省令」です。
しかし、製造販売業者の監督だけでなく、「製造」工程の現場においても問題が生じないようにする必要があるので、製造業者においても、一定の基準をクリアしなければ許可を得ることはできないものとされています。
そして、「製造」については、①きちんとした設備のある製造所であること(製造所の構造設備)と、②製造工程が適切な人的体制などで行われること(製造管理と品質管理)が求められます。
そのため、この2つの観点から、基準は、以下のように、厚生労働省の規則としてまとめられています。
① 製造所の構造設備に関する基準
=『薬局等構造設備規則』
② 製造における製造管理及び品質管理の基準
=『医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令』
(通称「GMP省令」=Good Manufacturing Practice)
(GMP省令の「M」は、Manufacturing=製造業の「M」なので理解は容易です)
イ 構造設備に関する基準
このうち①は、上記⑵で見た許可の区分ごとに、必要な設備が分けられています。精製する工程と保管する工程とで必要な設備が異なることから、当然の区分となります。本稿では詳細な説明は割愛いたしますが、その内容を見れば、医薬品という製品の特殊性から、非常に詳細な事項が要求されていることがお分かりになるかと思います。
ウ 製造管理及び品質管理の基準
(ア)2つの部門の独立と責任者
次に②は、製造における人的体制などについて定めていますが、基準の表題のとおり、製造管理と品質管理を別のものとしています。つまり、製造管理部門と品質管理部門を分け、相互に独立させることが求められており、製造販売業における総括製造販売責任者のように、この2部門を統括する責任者を設けることが必要になります。
この責任者を「医薬品製造管理者」といい、薬剤師の資格が必要になるので、一般的には「管理薬剤師」とも言われます。
(イ)SOPの作成とこれに基づく運用
以上のような部門と責任者の指揮のもと、医薬品の製造が行われますが、各部門における実際の作業やチェックの手順がしっかりと定まっていなければ、適切な製造はできません。そのため、作業内容を定めたマニュアルが必要になります。
GMP省令は、このマニュアルとして、「製造管理基準書」、「品質管理基準書」、「衛生管理基準書」、「製品標準書」、「教育訓練基準書」、「回収処理基準書」など、各部門や工程、対応が必要な場面ごとに必要な手順をまとめた多数のマニュアル作成を義務付けています。これらを総称して「SOP(Standard Operation Procedures)」と言います。
このように、製造工程においては、各人ごとのバラバラな対応になることなく、製造所全体で適切な製造がなされるように、マニュアルに基づく運用が求められています。
(ウ)試験検査の実施
上記のように、医薬品製造においては、マニュアルに基づく工程管理が行われますが、最終的な検査を行うことも義務付けられております。この検査は、製造管理部門ではなく品質管理部門が行い、ロットあるいは管理単位ごとになされます。最終的に、試験結果が文書で報告され、合格した場合に出荷されます。
なお、生物学的製剤などについては、製造業者内部の試験検査に加え、さらに国(国立感染症研究所)が検査を行うものとされています(薬機法第43条)。
医薬品が、極めて慎重な確認を経て製造されていることが分かります。
⑸ 不良医薬品
上記のように、医薬品の製造は、厳格な基準のもとで行われていますが、不良品が生じてしまうこともあります。
このため、当然のことですが、薬機法は、不良医薬品の販売・授与、その目的での製造・輸入・貯蔵・陳列を禁止しています(薬機法第56条)。
具体的には、以下の医薬品が「不良医薬品」となります。
薬機法第56条
1号~5号
日本薬局方や厚生労働大臣が定めた基準に適合しない医薬品
6号
不潔な物質、変質・変敗した物質から成っている医薬品
7号
異物が混入、付着している医薬品
8号
病原微生物その他疾病の原因となるものにより汚染され、又は汚染されているおそれがある医薬品
9号
認められないタール色素が使用されている医薬品
⑹ 外国製造業者の認定
前述のように、医薬品管理の責任は製造販売業が担う一方で、「製造販売」と「製造」が別々の概念であることはご説明しました。製造販売とは、品質管理と安全管理を担う立場なので、自ら医薬品を「製造」しなくてもよく、国内の外部業者に「製造」を委託してもいいですし、外国の業者が「製造」した製品を輸入してもよいことになっています。そして、この「製造」については、製造工程が適切になされるか確認する必要がありますので、別に「製造業の許可」(保管のみの一部については「製造業の登録」)が必要なこともご説明しました。
この確認は、日本国内の業者に限らず、外国の業者に対しても必要となります。もっとも、薬機法は日本の法律なので、外国の法律に服している外国の業者に対して、日本政府が「許可」や「登録」を認めることはできません。そのため、薬機法は、外国の製造業者に対しては、「許可」や「登録」に代わる制度として「認定」という制度を設けています。
6.医薬品の品質管理
最後に、製造販売業、製造業のいずれにも関わる「医薬品の品質管理」について見ていきます。
製造販売業のところで前述しましたように、製造販売業者に求められるのは、①医薬品の「品質管理」と②医薬品の「市場流通後の安全管理」の2つであり、それぞれGQP省令とGVP省令の2つの基準が定められています。
そして、この「品質管理」を行うために、製造販売業者では品質保証部門を設け、その責任者として「品質保証責任者」の設置が義務付けられており、医薬品の品質管理について最終責任を負うのは、製造業者ではなく、製造販売業者となります。
したがって、品質管理は、医薬品が製造されてから市場に流通するまでに限らず、流通後の情報収集や不良医薬品の回収などの全ての段階において行われることになります。
薬機法では、製造販売と製造は別の概念とされており、製造販売業者が自ら製造することもあれば、外部の製造業者に委託することもあります。ただし、製造がどのようなパターンであっても、この「製造」過程における最終的な品質管理を行うのは製造販売業者となります。製造業者は、製造工程における品質管理を行うものとされていますが、大きく言えば、製造販売業者の品質管理の中で、これを行っていることになります。基準のレベルでいえば、GMPはGQPによる管理・監督のもとで行われます。
7.まとめ
以上、今回は、医薬品が市場に流通する場面での規制のうち、主に、事業者に関する規制を見てきました。かなり多岐に渡る内容でしたが、特に重要なポイントは以下のとおりです。
・医薬品を市場に流通させるためには、以下の①②が必要となる
① 医薬品自体の製造販売承認
② 事業者の製造販売業許可
・薬機法における、製造販売、製造、販売の各言葉の違いを理解する
製造販売…医薬品を「市場流通」させること
製造 …医薬品を「製造」すること
販売 …「流通した医薬品を販売」すること
・製造販売業者は、「三役」を設置し、医薬品の「品質管理」と「市場流通後の安全管理」を行う
・製造業者は、担当する製造工程により許可の種類が異なる
・医薬品の品質管理は、製造販売業者の管理・監督のものとでなされる
次回は、医薬品自体の製造販売承認について解説いたします。
連載:薬機法とは ~薬機法の基本~
『第1回 薬機法の全体像』はこちらから
『第2回 「医薬品等」とは』はこちらから
『第3回 医薬品の販売と薬局 ① -医薬品の種類-』はこちらから
『第4回 医薬品の販売と薬局② -医薬品の販売と薬局-』はこちらから
『第6回 医薬品の製造販売② -医薬品の製造販売承認-』はこちらから
監修
弁護士 鈴木 景
(都内法律事務所からインハウスローヤーを経て、2017年GVA法律事務所入所。 スタートアップから大手上場企業まで、新規事業開発支援、契約書作成レビュー支援、株式による資金調達、M&AやIPOによるExitの支援など幅広く対応。 対応領域も、医療・美容に関する広告規制対応や、食品関連ビジネス、旅行関連ビジネス、NFT関連ビジネスと幅広い。)